H2so4 Lewis Säure
Die Lewis- oder Brönstedt-Säure-katalysierte Veresterung einer Carbonsäure mit einem Alkohol zu Ester und Wasser ist eine typische Gleichgewichtsreaktion. Nach der Lewis-Theorie ist eine Säure ein Teilchen das über ein leeres äußeres Orbital verfügt das zur Bildung einer kovalenten Bindung ein Elektronenpaar aufnehmen kann.
![]()
Saure Base Theorie Nach Lewis In Chemie Schulerlexikon Lernhelfer
Es ist also eine chemische Verbindung mit der Möglichkeit ein Elektronenpaar aufzunehmen.
H2so4 lewis säure. Eine Lewis-Base ist dementsprechend ein Elektronenpaardonator der Elektronenpaare abgeben kann. BH3 SiF4 AlCl3 SnCl4 etc. Schwefelsäure H2SO4 Schwefelsäure nach IUPAC -Nomenklatur Dihydrogensulfat veraltet Vitriolöl ist eine chemische Verbindung des Schwefels mit der Summenformel H 2 SO 4.
H 2 SO 4 HNO 3 NH 4 sind keine Lewis Säuren Beispiele für Säure - Base - Reaktionen. H2SO4 brauner Ring von FeH2O5NO2 CO3 2-. A Ansäuern mit HNO3 Zugabe von NH46Mo7O24.
NH3g H2O l NH4 aq Cl-aq Das Wassermolekül ist hier die Säure da es ein Proton abgibt das vom Ammoniakmolekül als Base aufgenommen wird. Bei organischen Säuren wenn mehr als eine saure Gruppierung vorhanden ist. Nach dem Lewis-Säure-Base-Konzept handelt es sich bei einer Lewis-Säure um einen elektrophilen Elektronenpaarakzeptor.
B OH3 H2O B OH4- und H. A H 2 OH 3 O d H 2 AsO 4 H 3 AsO 4 b HS H 2 Se F HF c NH 3 NH 4 f NO 2 HNO 2. Dementsprechend wirkt Borsäure als Säure.
A Säuren sind nach dem Konzept von Brønsted Protonen-Donatoren 1 Säuren sind nach dem Konzept von Lewis Elektronen-Akzeptoren 1. Eine Lewis-Säure ist eine Säure die unabhängig von der Fähigkeit definiert ist Protonen aufzunehmen und abzugeben. Eine Lewis-Säure besitzt also eine Elektronenpaarlücke die mit Bindungselektronen besetzt werden kann.
HNO3 Gasentwicklung prüfen mit BaOH2 Barytwasser auf CO2 PO4 3-. Dazu gehören die Elemente Kohlenstoff Stickstoff Sauerstoff Fluor Natrium Magnesium und Aluminium. H2SO4 2 NH3 2 NH4 SO42 2 mol 1 mol nH2SO4 1 g 98gmol 198 mol nNH3 298 mol 298 mol 17 gmol 0347 g 2019 In 1 L eines Acetat-Puffers liegen 01 mol Natriumacetat und 05 mol Essigsäure pKS.
Im ersten Schritt gibt die Schwefelsäure oder auch eine andere Säure ein Proton an das Carbonyl-O-Atom der Carbonsäure ab. Ansäuern mit 1m H2SO4 Zugabe von frischer FeSO4-Lsg Unterschichten mit konz. Geben Sie je ein Beispiel an für eine.
Dreiprotonig Bei organischen Säuren wenn mehr als eine saure Gruppierung vorhanden ist. Nach Erhitzen gelber Nd PMo3O1043-. Sondern eine Säure - Base - Reaktion s.
A H 3 PO 4 H 2 PO 4 d HS S2 b H 2 PO 4 HPO 2 4 e H 2 SO 4 HSO 4 c NH 3 NH 2 f HCO 3 CO 2 3 3WelcheistdiekonjugierteSäurevon. Reaktion zwischen Ammoniak und Wasser. Molekulare Lewis Säuren die stärker als.
Lewis-Säure Eine Lewis-Säure ist nach dem Säure-Base-Konzept von G. Auch hier muss eine che- mische Reaktion zwischen den Ammoniakmolekülen NH3 und den Wassermolekülen H2O statt- gefunden haben. Die Oktettregel gilt streng nur für die Hauptgruppenelemente ohne Wasserstoff und Helium.
Lewis ein elektrophiler Elektronenpaarakzeptor kann also Elektronenpaare anlagern. EPA EPD º Substrat Säure-Base-Komplex H Cl-º HCl OCO O2-º CO 3 2-H NH 3 º NH 4 Men Hx 2. Periode gehorchen nicht mehr der Oktettregel was bei Strukturen zur Oktetterweiterung führt - siehe Beispiel Schwefelsäure H2SO4Ein Ü.
HCl HNO3 H2SO4 z. U 11 Lewis - Konzept. Analog zu den Brønstedt Supersäuren diejenigen die stärker als 100 H2SO4 sind wurde in dieser Arbeit der Begriff Lewis Supersäure definiert.
Also Borsäure gibt gar keine Protonen ab es ist eine Säure und zwar eine sogenannte Lewis-Säure es wirkt also als Elektronenpaarakzeptor. Dies ist eine einfache Säure-Base-Reaktion eine Protolyse sowohl nach Brönsted. Ursubstanz mit HCl od.
Sie ist eine farblose ölige sehr viskose und hygroskopische Flüssigkeit. Schwefelsäure wirkt stark ätzend und ist eine der stärksten Mineralsäuren.

Elektrophile Aromatische Substitution Wikipedia
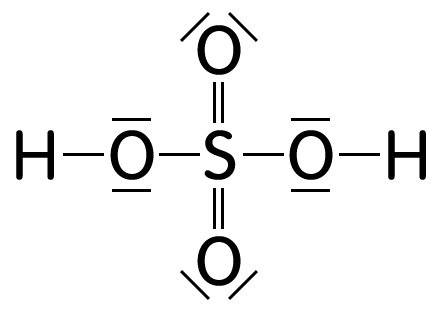
Eqiooki De Chemie Schwefelsaure
Chemisches Rechnen Ii Schwache Sauren Ph Und Pks Sauren Und Basen Chemie Sek Ii
Chemie Der Nichtmetalle Kap 5 5
Https Www Chemie Uni Hamburg De Studium Chemie Im Nebenfach C082 Vorlesung 082 Inhalt Nebenfach Ac Handout Pdf

Oktetterweiterung Einfuhrungsvideo Schwefelsaure Youtube
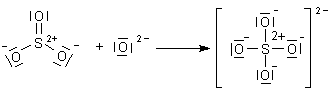
Prof Blumes Medienangebot Schwefel Das Exemplarische Nichtmetall
Chemie Der Nichtmetalle Kap 5 5
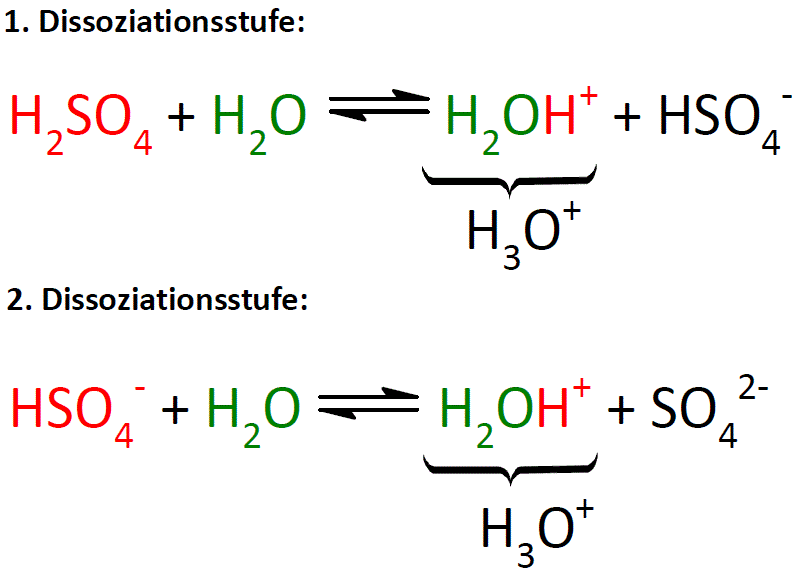
Mehrprotonige Sauren Anorganische Chemie
Https Www Uni Marburg De Fb15 Studium Praktika Nebenfach Bioprakt Biouebung7loesung

Schwefelsaure Formel Leicht Erklart I Ubungen

Chemie Elektrophil Tabelle Schule Chemieunterricht Organische Chemie

Schwefelsaure Formel Leicht Erklart I Ubungen
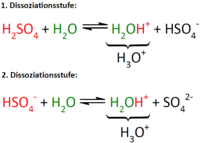
Mehrprotonige Sauren Anorganische Chemie
Https Www Chemie Uni Hamburg De Studium Chemie Im Nebenfach C082 Vorlesung 082 Inhalt Nebenfach Ac Handout Pdf

